Descrizione
Anatomia
Complicanze
Fattori di rischio
Diagnosi e screening
PSA
Esplorazione digito-rettale (EDR)
Devo essere sottoposto allo screening?
Sintomi
Diagnosi
Stadiazione
Terapia
Sorveglianza attiva
Chirurgia
Radioterapia
Terapia alternativa
Terapia ormonale
Chemioterapia
Descrizione (torna su)
Il tumore alla prostata è una patologia caratterizzata dalla proliferazione incontrollata delle cellule prostatiche. Il cancro alla prostata, se diagnosticato e trattato precocemente, ha un tasso di guarigione superiore al 90%. Oggi giorno infatti esistono svariate efficaci opzioni di trattamento per questo tipo di tumore. Tuttavia, ciascuna di queste opzioni terapeutiche è caratterizzata da specifici benefici e complicanze. È molto importante che un paziente che riceve una diagnosi di tumore alla prostata si rivolga ad un urologo esperto ed obiettivo che lo affianchi e lo consigli nella maniera più appropriata per la scelta del miglior trattamento possibile. Tale trattamento deve essere commisurato alla gravità della malattia e personalizzato in base ad ogni specifico caso clinico.
Una volta diagnosticato, il tumore alla prostata è una malattia in grado di determinare modifiche sostanziali nella vita di una persona. Ogni paziente si troverà nella condizione di prendere delle decisioni riguardanti i possibili trattamenti, le cui conseguenze possono ripercuotersi drasticamente sia sulla propria vita che su quella dei suoi familiari. Ogni anno in Italia viene diagnosticato un tumore alla prostata in più di 70mila uomini: ciascuno di questi dovrà prendere decisioni molto personali ed individualizzate riguardo le opzioni di trattamento e subire modifiche del proprio stile di vita.
Questo sito internet si prefigge l’arduo compito di aiutare i pazienti e le loro famiglie a comprendere come si sviluppa il tumore alla prostata, quali sono i suoi fattori di rischio, come viene diagnosticato e passa in rassegna tutte le possibili opzioni di trattamento.
Anatomia (torna su)
La prostata è una ghiandola avente la forma simile ad una castagna. Si trova sotto la vescica e davanti al retto. L’uretra, il condotto che trasporta sia l’urina che lo sperma, decorre per un suo tratto all’interno della prostata. Il retto si trova appena dietro la prostata e la vescica. Dietro e poco superiormente alla prostata sono ubicate le vescicole seminali, due piccole ghiandole che secernono circa il 60% delle sostanze che compongono lo sperma. Lateralmente alla prostata decorrono i nervi che controllano la funzione erettile.
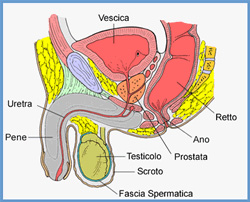
si notino i rapporti della prostata
con la vescica, con il retto e con l’uretra.
Possibili complicanze di un trattamento radicale (torna su)
Nonostante il progresso della tecnologia, tutte le opzioni di trattamento per il tumore alla prostata sono tutt’oggi gravate da possibili effetti collaterali: non esiste allo stato attuale nessuna forma di terapia che garantisca al paziente l’assoluta certezza della guarigione completa associata all’assenza di complicanze. Le possibili complicanze di un trattamento radicale per il cancro alla prostata incidono in maniera molto negativa sulle funzioni sessuali, urinarie ed intestinali.
In condizioni normali, la continenza dell’urina è determinata dagli sfinteri urinari.
Gli sfinteri sono delle strutture muscolari che contraendosi impediscono all’urina raccolta nella vescica di fuoriuscire. Esistono due sfinteri urinari: uno alla base della vescica ed uno a livello dell’apice prostatico. Gli sfinteri devono rimanere contratti per assicurare la continenza, mentre durante la minzione si rilasciano consentendo il passaggio dell’urina dalla vescica all’esterno del corpo.
Sia un trattamento chirurgico che un trattamento radioterapico possono ledere gli sfinteri urinari causando incontinenza (perdita urinaria involontaria). Inoltre, durante la prostatectomia, il chirurgo urologo, dopo aver rimosso la prostata, deve confezionare una anastomosi uretro-vescicale, ossia deve ricongiungere l’uretra residua al collo vescicale. Questo passaggio è molto delicato, dal momento che, se non eseguito alla perfezione, si può verificare una “stenosi dell’anastomosi”, ossia una ostruzione al passaggio dell’urina. Questa complicanza ha conseguenze molto negative ed invalidanti sulla vita dei pazienti. Una possibile conseguenza della radioterapia è il danneggiamento del retto, che può determinare diarrea, urgenza rettale ed incontinenza fecale (perdita involontaria di feci). Altra temibile complicanza è la disfunzione erettile, ossia la incapacità di raggiungere e/o mantenere una rigidità del pene soddisfacente per svolgere un rapporto sessuale completo. La causa della disfunzione erettile è la lesione dei nervi erigendi che decorrono molto vicini alla prostata. Tali nervi possono essere danneggiati sia dalla chirurgia che dalla radioterapia. Come conseguenza, il paziente continuerà ad avere il desiderio sessuale ma sarà impossibilitato a raggiungere una erezione. Inoltre, sia la chirurgia che la radioterapia causano infertilità.
Fattori di rischio (torna su)
Il tumore alla prostata è il tipo di tumore più frequente nel sesso maschile: in Italia un uomo su otto ne è affetto. L’incidenza dell’adenocarcinoma prostatico aumenta con l’età. Al di sotto dei 40 anni l’incidenza di questo tumore è di 1/10.000 ma si eleva a 1/ 38 per la fascia di età tra i 40 ed i 59 anni e di 1/14 per i pazienti di età compresa tra i 60 ed i 69 anni. Nel 65% dei casi di cancro alla prostata colpisce gli uomini di età’ maggiore di 65 anni.
I principali fattori di rischio del cancro alla prostata sono l’ereditarietà e la razza. Gli individui di razza africana hanno una probabilità del 61% maggiore rispetto a quelli di razza caucasica di sviluppare un tumore alla prostata ed hanno un rischio di morire di questa malattia quasi 2 volte e mezzo superiore. Gli uomini che hanno un parente di primo grado (padre, fratello o figlio) con una storia di tumore alla prostata hanno una probabilità due volte superiore di sviluppare questa patologia, mentre per quelli con due o più parenti questo rischio si quadruplica. Il rischio è ancora maggiore se i familiari affetti ricevono la diagnosi in giovane età. Anche se la genetica riveste un ruolo fondamentale, anche fattori sociali ed ambientali, come la dieta e lo stile di vita hanno la loro importanza.
Infatti, studi recenti hanno dimostrato che la modifica della dieta può diminuire sia l’incidenza che rallentare la progressione del tumore alla prostata. Esistono inoltre dei fattori che non sono correlati all’ insorgenza del tumore alla prostata. Malattie molto comuni come la IPB (iperplasia prostatica benigna) e la prostatite, pur causando sintomi simili a quelli del carcinoma prostatico e che rientrano sempre nelle specifiche competenze dell’urologo, non sono mai state messe in correlazione col rischio di sviluppare un tumore alla prostata. Assolutamente falsa è anche l’ipotesi che una intensa vita sessuale e l’avere frequenti eiaculazioni possano aumentare il rischio di tumore alla prostata. Al contrario, alcuni studi hanno dimostrato che una vita sessuale intensa abbia invece un ruolo protettivo.
Prevenzione
Nonostante il progresso scientifico allo stato attuale non sono disponibili strategie di prevenzione per il cancro alla prostata. Una certa efficacia è stata dimostrata per la finasteride e la dutasteride, due farmaci usati per la terapia della IPB.
Diagnosi e screening (torna su)
Lo scopo di un programma di screening è quello di diagnosticare una determinata malattia in uno stadio precoce, prima che i suoi sintomi si manifestino. Il cancro alla prostata può essere trattato in maniera molto più efficace se viene diagnosticato in uno stadio iniziale. Lo screening del carcinoma prostatico viene eseguito in maniera semplice e rapida da un esperto urologo sulla base di due elementi diagnostici: l’analisi del sangue del PSA (antigene prostato-specifico) e l’esplorazione digito-rettale (EDR).
PSA (torna su)
Il PSA è un enzima prodotto dalle cellule prostatiche che espleta la funzione di scindere dei legami chimici nel liquido seminale. Questo enzima ha un importante ruolo per la fertilità maschile. Il PSA è prodotto solo dalla prostata ed una sua elevazione nel sangue indica inequivocabilmente la presenza di una patologia prostatica. Tuttavia, il PSA aumenta indistintamente in tutte le malattie della prostata: ipertrofia, prostatite e tumore. Pertanto, basandosi solo sulla valutazione del PSA non è possibile stabilire con precisione quale patologia di fondo ha determinato un aumento di questo marcatore nel sangue. Il livello del PSA inoltre è influenzato anche dalle dimensioni della prostata.
Il PSA viene dosato nel sangue in nanogrammi per millilitro (ng/ml). Un valore di PSA inferiore ai 4 ng/ml è considerato nella norma, un valore tra 4 e 10 ng/ml è considerato sospetto, mentre un valore superiore a 10 è molto sospetto per la presenza di un tumore. Nei due terzi dei casi, eseguendo una biopsia prostatica, non viene diagnosticato un tumore negli individui che presentano livelli di PSA compresi tra 4 e 10. Tuttavia, è importante sottolineare, che è possibile diagnosticare un tumore alla prostata anche in casi di livelli di PSA inferiori a 4 ng/ml. Livello di PSA molto elevati indicano con buone probabilità la presenza di un tumore alla prostata.
Da quanto scritto si può facilmente comprendere che la valutazione del solo valore del PSA non e’ attendibile al 100 %. Per questo,quando il livello di PSA è alto, è indispensabile eseguire una biopsia della prostata per confermare od escludere la presenza di un tumore alla prostata. Per aumentare la specificità del PSA è inoltre possibile utilizzare i suoi derivati quali il rapporto tra il PSA libero ed il totale. Il PSA circola nel sangue in due diverse forme: libero o legato alle proteine del sangue. Il PSA totale è la somma di ambedue queste forme mentre il PSA libero e’ relativo solo alla quota non legata alle proteine.
Alcuni studi hanno dimostrato che le cellule prostatiche tumorali producono PSA in forma legata alle proteine: quindi, una quota più bassa di PSA libero rispetto al PSA totale è sospetta per un adenocarcinoma prostatico. Invece, un’alta percentuale di PSA libero rispetto al PSA totale fa propendere per una ipertrofia prostatica. Il valore del rapporto tra il PSA libero ed il totale si esprime tramite una percentuale (Rapporto PSA libero/PSA totale per 100): tale rapporto viene solitamente considerato nella norma nella pratica clinica quando è superiore al 20%. Tuttavia non è infrequente diagnosticare un carcinoma prostatico anche quando il rapporto tra il PSA libero ed il totale è maggiore del 20% oppure avere un riscontro di infiammazione della prostata per valori inferiori. Pertanto, anche il rapporto tra il PSA libero e totale non è un parametro affidabile al 100%, ma rappresenta comunque un utile strumento nelle mani di un esperto urologo per diagnosticare una malattia della prostata. Altri derivati del PSA sono la “PSA velocity” che misura la velocità con cui cresce il PSA nel tempo e la “PSA density” che rappresenta il rapporto tra valore del PSA e volume della prostata misurato tramite ecografia.
Esplorazione digito-rettale (EDR) (torna su)
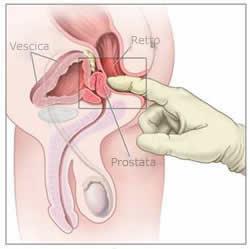
L’esplorazione rettale è un esame semplice e rapido. Tramite l’introduzione nel retto del paziente del dito indice coperto da un guanto e lubrificato, l’urologo riesce a valutare le caratteristiche della prostata (volume, superficie, forma, consistenza). La prostata sana ha una consistenza molle, come la zona della mano tra palmo ed il pollice.
Un tumore alla prostata è duro, asimmetrico e, nei casi avanzati, di consistenza simile alla pietra. Se all’esplorazione rettale si sospetta la presenza di un tumore, si pone l’indicazione all’ esecuzione di esami diagnostici supplementari come la biopsia prostatica.
Devo essere sottoposto allo screening?(torna su)
La società europea di urologia consiglia di eseguire un’analisi annuale del PSA a partire dai 50 anni. Gli individui considerati ad alto rischio (storia familiare positiva e individui di razza nera) dovrebbero iniziare i controlli di screening a partire dai 45 anni. Altri individui a rischio sono i soggetti il cui valore di PSA a 40 anni è superiore ad uno. Tali individui dovrebbero eseguire un dosaggio del PSA ogni due anni dai 40 ai 50 anni ed annualmente dopo i 50 anni.
Lo screening del PSA è tutt’ oggi un argomento molto dibattuto e non vi è una accordo unanime riguardo i suoi benefici. I favorevoli sostengono che lo screening consenta di diagnosticare e curare l’adenocarcinoma prostatico in uno stadio molto precoce, offrendo al paziente più opzioni di trattamento. I contrari, invece, ritengono che, considerato il fatto che la maggior parte dei tumori della prostata si sviluppa molto lentamente e non ha un carattere aggressivo, in un numero cospicui di casi gli effetti secondari del trattamento superino i benefici derivanti dalla diagnosi precoce.
Sintomi (torna su)
Nella fase iniziale del tumore alla prostata, la maggior parte dei uomini non avverte alcun sintomo. In alcuni casi, tuttavia, possono essere presenti uno o più dei seguenti sintomi:
- Stimolo frequente di urinare, particolarmente durante la notte
- Difficoltà a ritardare la minzione
- Bruciore urinario
- Problemi di erezione
- Eiaculazione dolorosa
- Sangue nell’urina e/o nello sperma
È bene sottolineare che tutti questi sintomi sono aspecifici e possono dipendere anche da altre malattie. Pertanto è fondamentale rivolgersi ad un esperto urologo per ricevere una precisa diagnosi.
Diagnosi (torna su)
La metodica fondamentale per la diagnosi dell’adenocarcinoma prostatico è la Biopsia prostatica. Tramite questo esame, eseguito sotto guida ecografica, si utilizza un sottile ago per prelevare dei piccoli campioni di tessuto prostatico. La biopsia prostatica pur comportando piccolo disagi, viene effettuata in regime ambulatoriale.
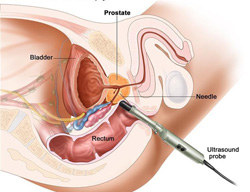
preleva campioni di tessuto prostatico
Classificazione di Gleason
In condizioni normali, le cellule prostatiche, similmente alle altre cellule del nostro corpo, si riproducono e muoiono di continuo. Ogni nuova cellula della prostata che viene generata nel normale ciclo di riproduzione cellulare ha la stessa forma e le stesse dimensione delle altre.
Le cellule tumorali hanno invece un aspetto differente. Il grado del tumore indica quanto le cellule tumorali sono differenti dalle cellule normali. Le cellule tumorali di “basso grado” sono molto simili al loro corrispettivo normale, mentre le cellule di “alto grado” hanno un aspetto completamente differente.
Il sistema di classificazione di Gleason include cinque diversi gradi che indicano il grado di differenziazione cellulare, ossia quanto le cellule tumorali differiscano dal loro corrispettivo normale. Il grado 1 indica che le cellule prostatiche tumorali hanno un aspetto molto simile alle cellule normale, mentre il grado 5 sta a significare che le cellule hanno un aspetto completamento differente.
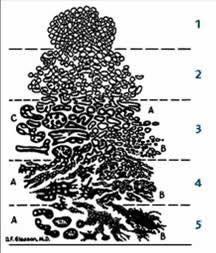
Il medico che esamina i campioni di biopsia prostatica si chiama anatomo-patologo, o semplicemente patologo. È proprio il patologo il medico che attribuisce al campione di biopsia prostatica il grado di Gleason. Per ogni biopsia vengono assegnati due gradi Gleason, uno relativo al grado Gleason del modello cellulare più frequente nel campione e un secondo grado di Gleason al secondo modello più frequente. I due gradi vengono sommati costituendo così un punteggio (“Gleason Score”) che può variare da un minimo di 2 (meno maligno) a un massimo di 10 (più maligno). Il “Gleason score” è nella maggior parte dei casi in grado di predire l’aggressività della malattia. Più alto è il “Gleason score”, meno cellule si comportano come cellule normali, e più il tumore tende ad essere aggressivo.
Stadiazione (torna su)
La stadiazione (in inglese “staging”) determina quanto un tumore alla prostata si è’ diffuso nel corpo. Tumore localizzato o anche detto “organo-confinato” sta a significare che il tumore è delimitato all’ interno dalla capsula prostatica, ossia è limitato all’interno della ghiandola. Tumore localmente avanzato indica che il tumore è per la maggior parte contenuto all’interno della prostata, ma ha parzialmente cominciato a diffondersi ai tessuti immediatamente circostanti. Nella malattia metastatica, il tumore si è diffuso al di fuori dell’organo e dei tessuti circostanti interessando organi più distanti.
La stadiazione della malattia si basa sullo svolgimento di precisi esami diagnostici quali l’ecografia transrettale, la TAC e la risonanza magnetica nucleare (RMN). Tuttavia, nessuno di questi esami ha una precisione diagnostica affidabile al 100%. L’unico esame che può affermare con certezza se un tumore è limitato alla prostata o se è sconfinato al di fuori dei suoi limiti anatomici è l’esame istologico definitivo, ossia lo studio dell’organo sezionato effettuato al microscopio da un anatomo-patologo dopo la rimozione chirurgica.
I linfonodi pelvici sono alcuni degli organi vicini alla prostata che possono essere interessati dalla diffusione metastatica delle cellule prostatiche tumorali. Questo avviene perché le cellule tumorali diffondono tramite il sistema linfatico, un sistema circolatorio simile a quello sanguigno che trasporta le cellule che combattono le infezioni. Nel corso di un intervento chirurgico di prostatectomia, i linfonodi vengono rimossi e successivamente esaminati per determinare la presenza di cellule tumorali. Conoscere lo stadio dell’adenocarcinoma prostatico è fondamentale per determinare quanto aggressivamente la malattia deve essere trattata, potendo scegliere tra diverse opzioni di trattamento disponibili.
Terapia (torna su)
Per il cancro alla prostata sono disponibili varie opzioni di trattamento, ognuna delle quali è caratterizzata da una diversa aggressività, invasività ed incidenza di effetti collaterali. Pertanto, e’ fondamentale che ogni paziente venga informato dettagliatamente riguardo le varie opzioni terapeutiche al fine di potere prendere la sua personale decisione opportunamente consigliato dal proprio urologo di fiducia.
Tale decisione si basa prevalentemente su una combinazione di fattori clinici e psicologici. Nella maggior parte dei casi un individuo a cui viene diagnosticato un carcinoma prostatico ha una lunga aspettativa di vita, pertanto la decisione terapeutica rivestirà una fondamentale importanza ed i suoi effetti avranno importanti conseguenze.
Sorveglianza Attiva (torna su)
Quando un tumore alla prostata viene diagnosticato in uno stadio molto iniziale, gli effetti collaterali di un trattamento radicale superano i benefici. Si stima che circa il 45% degli individui in cui, grazie allo screening con il PSA, il tumore alla prostata viene diagnosticato in uno stadio iniziale, sono candidati alla sorveglianza attiva. I pazienti che scelgono questa opzione, vengono sottoposti ad una stretta sorveglianza medica: il trattamento radicale viene instaurato quando vi sono segni che il tumore possa divenire potenzialmente pericoloso per l’aspettativa di vita del paziente.
L’obiettivo della sorveglianza attiva è proprio quello di stabilire con esattezza la tempistica con cui iniziare un trattamento curativo. Infatti, i pazienti che scelgono la sorveglianza attiva non si sottopongono subito ad un trattamento radicale quale un intervento chirurgico o la radioterapia, ma scelgono di rimandarlo il più tardi possibile, evitando in questo modo anche le complicanze ed i costi legati ad un trattamento radicale. La sorveglianza attiva si basa su un attento controllo del paziente volto ad individuare segni di progressione del tumore. Ogni sei mesi si effettuano un dosaggio del PSA ed una visita urologica con esplorazione rettale e viene eseguita annualmente una biopsia prostatica. Il trattamento curativo, chirurgico o radioterapico, viene prontamente eseguito se dai controlli si evince una progressione del tumore.
La sorveglianza attiva è sicuramente una ottima scelta sia per i pazienti affetti da tumori poco aggressivi (basso Gleason score) e diagnosticati in uno stadio iniziale che per i pazienti in precarie condizioni generali affetti da altre patologie più gravi dell’adenocarcinoma prostatico. Un trattamento radicale per il tumore alla prostata può comportare svariati effetti collaterali come la disfunzione erettile e problemi urinari: tali complicanze sono difficili da tollerare per individui in buona salute. Inoltre, se un paziente è affetto contemporaneamente da altre malattie, quali patologie cardiache o diabete scompensato, l’urologo potrà consigliare di non effettuare alcun trattamento ed evitare le relative potenziali complicanze.
Chirurgia (torna su)
Il trattamento chirurgico consiste nella prostatectomia radicale, ossia la completa rimozione della prostata e delle vescicole seminali. Viene eseguito nella fase precoce della malattia quando il tumore è ancora confinato alla prostata. Il tipo di prostatectomia più frequentemente eseguito è la prostatectomia radicale retro pubica. Durante questa operazione, viene praticata una piccola incisione addominale tra ombelico e pube attraverso la quale la prostata viene rimossa dalla sua collocazione anatomica dietro l’osso pubico. Dopo la rimozione della prostata, il chirurgo urologo sutura l’uretra direttamente con la vescica (anastomosi uretro-vescicale) in modo da ristabilire una normale minzione. Per la guarigione della anastomosi sono necessari alcuni giorni, pertanto viene posizionato un catetere vescicale per consentire il deflusso spontaneo dell’urina. Tale catetere rimane solitamente per circa 10 giorni.
La prostatectomia radicale perineale è un altro tipo di intervento chirurgico, effettuato meno frequentemente. Durante questa procedura il chirurgo urologo rimuove la prostata eseguendo un’incisione sul perineo, lo spazio compreso fra lo scroto e l’ano.
La prostatectomia laparoscopica prevede l’esecuzione di piccole incisioni addominali attraverso le quali il chirurgo urologo inserisce gli strumenti ed una telecamera. L’ intervento viene eseguito senza aprire l’intero addome e prevede le stesse fasi e le stesse modalità dell’operazione eseguita con accesso retropubico.
Nella laparoscopia tradizionale, è direttamente il chirurgo a manovrare gli strumenti laparoscopici; nella laparoscopia robot-assistita invece il chirurgo manovra dei bracci robotici attraverso una console.
La “nerve-sparing” è un tipo di tecnica chirurgica attraverso la quale la prostata viene rimossa risparmiando i nervi erigendi che decorrono lateralmente ad essa. Questa tecnica, che viene eseguita al fine di conservare l’erezione del paziente, non è praticabile nei casi più avanzati in cui il tumore si diffonde oltre la ghiandola. È possibile eseguire una tecnica nerve sparing sia tramite accesso retro pubico che laparoscopico.
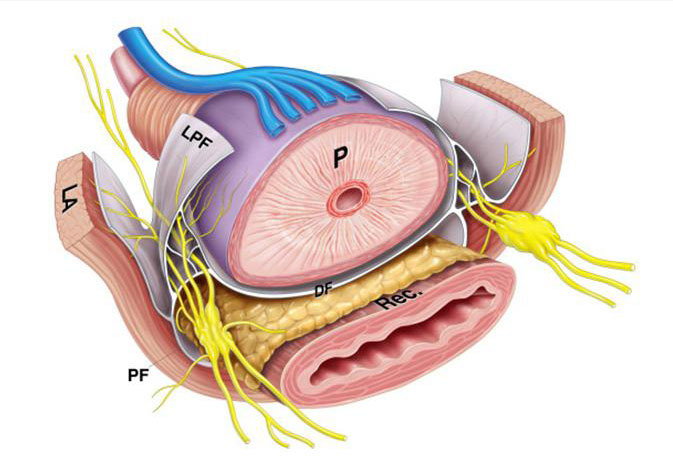
Si noti il loro decorso molto vicino alla prostata
A prescindere dal tipo di tecnica chirurgica, la prostatectomia è gravata dalle seguenti possibili complicanze:
- Disfunzione erettile
- Incontinenza urinaria
- Stenosi dell’anastomosi uretro-vescicale con conseguente difficoltà ad urinare
- Emorragia intraoperatoria
Importanza dell’abilità chirurgica
A prescindere dal tipo di tecnica utilizzata, sia essa retro pubica o laparoscopica, la prostatectomia è un intervento di difficile esecuzione i cui risultati sono strettamente connessi all’abilità ed all’ esperienza del chirurgo. Pertanto risulta fondamentale la scelta di un chirurgo esperto che opera in una struttura adeguata.
Ultimamente la tecnica robotica viene propagandata come il miglior tipo di trattamento chirurgico. Tuttavia, recenti studi che hanno analizzato migliaia di casi hanno dimostrato che la prostatectomia robotica aumenta esponenzialmente i costi dell’intervento senza presentare alcuna superiorità in termini di risultati oncologici e funzionali rispetto alla tecnica retro pubica tradizionale.
Il costo di una prostatectomia robotica può arrivare fino a 100.000 euro, tuttavia, il dispendio di questa grossa somma di denaro non assicura affatto il buon esito dell’intervento. La prostatectomia robotica è gravata dalla stessa incidenza di complicanze della prostatectomia retro pubico tradizionale.
Radioterapia (torna su)
La radioterapia si prefigge lo scopo di “uccidere” le cellule tumorali mediante l’utilizzo delle radiazioni. La radioterapia può essere impiegata come trattamento curativo ad intento radicale, per le recidive dopo trattamento chirurgico e per la terapia palliativa dei tumori avanzati. Il tipo più comune di radioterapia è la radioterapia esterna conformazionale. Prima di effettuare un trattamento radioterapico, si esegue una TAC e/o una risonanza magnetica per individuare la posizione della ghiandola prostatica al fine di indirizzare le radiazioni nella corretta zona di trattamento. Dopodiché un programma computerizzato gestisce l’emissione delle radiazioni verso la zona da trattare in modo da intensificare le dosi nella posizione corretta.
La radioterapia ad intensità modulata (IMRT) permette di modulare l’intensità delle radiazioni diminuendo le dosi nelle zone adiacenti alla vescica ed al tessuto rettale al fine di ridurre gli effetti collaterali.
Con le tecniche di radioterapia più moderne si riescono a ridurre i danni derivanti dall’ irradiazione degli organi sani circostanti la prostata. A prescindere dal tipo di radioterapia esterna, solitamente vengono svolte circa 30 sedute dilazionate nel tempo in modo da diluire la dose delle radiazioni.
La brachiterapia è una tecnica che consiste nell’introdurre nella prostata dei piccoli semi contenenti iodio o palladio radioattivi. Questi semi vengono inseriti attraverso il perineo tramite dei piccoli aghi metallici. Come nella radioterapia conformazionale tridimensionale esistono programmi molto precisi che vengono impiegati per controllare la corretta disposizione dei semi all’interno della prostata. Nell’arco di molti mesi i semi emanano delle radiazioni nelle zone immediatamente circostanti causando la morte delle cellule tumorali.
Dopo un anno il materiale radioattivo si degrada ed i semi che rimangono diventano innocui.
Paragonata alla radioterapia esterna, la brachiterapia è meno frequentemente usata. Questa tecnica ha comunque il vantaggio di essere eseguita in una singola seduta di trattamento.
A prescindere dal tipo, la radioterapia può avere le seguenti complicanze ed effetti collaterali:
- Disfunzione erettile
- Incontinenza urinaria
- Infiammazione persistente della vescica (cistite post-attinica)
- Infiammazione persistente del retto (proctite post-attinica)
- Difficolta’ ad urinare
Importanza della pianificazione della dose
Come l’abilità chirurgica svolge un ruolo importante per la prostatectomia, così l’abilità tecnica è altresì necessaria per il buon esito della radioterapia. L’uso di software specifici e di computer agevola notevolmente tale compito, ma, alla fine, l’esperienza e l’abilità del radioterapista sono di cruciale importanza per il buon esito del trattamento. Pertanto è opportuno scegliere un radioterapista esperto che lavora in una struttura specializzata.
Chirurgia o Radioterapia?
Entrambe le opzioni di trattamento sono ampiamente utilizzate in tutto il mondo per la terapia del carcinoma prostatico. I risultati sono soddisfacenti per entrambe le metodiche soprattutto negli stadi precoci, mentre la chirurgia si è dimostrata superiore alla radioterapia per le forme più avanzate del carcinoma prostatico. Le complicanze, come già detto, sono strettamente connesse alla esperienza del centro presso cui viene eseguito il trattamento.
La radioterapia risulta psicologicamente più difficile da accettare per il paziente dal momento che la ghiandola prostatica non viene asportata e pertanto non può essere dettagliatamente esaminata per rilevare il grado e lo stadio del tumore. Inoltre, mentre la radioterapia può essere praticata a scopo adiuvante dopo la rimozione chirurgica (per rinforzarne gli effetti), una prostatectomia eseguita dopo un trattamento radiante è un intervento estremamente complesso e gravato da un alto tasso di complicanze.
Terapia alternativa (torna su)
La chirurgia e la radioterapia rappresentano oggigiorno il trattamento standard per il tumore alla prostata. Tuttavia esistono altre opzioni di trattamento meno diffuse ma che hanno dimostrato una certa efficacia. La Crioterapia, anche conosciuta come criochirurgia o crioablazione, è un tipo di trattamento praticato già da diversi anni. Tramite questa procedura vengono inserite delle sonde nella prostata attraverso il perineo (lo spazio compreso fra lo scroto e l’ano).
Successivamente vengono introdotti un gas contenente argon o azoto liquido al fine di determinare la morte delle cellule prostatiche tumorali per congelamento. Nel corso degli anni, sono state apportate varie migliorie tecniche per migliorare i risultati di questa procedura e per ridurne gli effetti collaterali, tuttavia, sia i tassi di disfunzione erettile che quelli di incontinenza urinaria rimangono alti ed i risultati oncologici non sono sovrapponibili a quelli della chirurgia e della radioterapia.
L’ HIFU (ultrasuoni focalizzati ad alta intensita’) ha un meccanismo di azione opposto alla crioterapia. Tramite questa procedura, le cellule della prostata muoiono per il riscaldamento. Viene inserita nel retto del paziente una sonda che genera ultrasuoni che vengono indirizzati verso la prostata. Anche l HIFU, così come la crioterapia, ha ottenuto dei risultati inferiori rispetto alla chirurgia e alla radioterapia. Tuttavia, sia l’HIFU che la crioterapia, sono tornate alla ribalta negli ultimi tempi perché sono attualmente utilizzate nella Terapia focale. La Terapia focale è un tipo di trattamento dell’adenocarcinoma prostatico che si prefigge l’obiettivo di distruggere il singolo focolaio tumorale all’ interno della prostata lasciando intatto l’organo circostante.
Questo tipo di terapia è praticabile nei casi molto precoci di tumore prostatico. Oltre che la crioterapia e l’HIFU anche altre metodiche possono essere utilizzate per eseguire una terapia focale: il trattamento fotodinamico, la vaporizzazione laser, la brachiterapia e il CyberKnife.
L’obiettivo principale della terapia focale è quello di limitare al massimo le complicanze. L’arruolamento dei pazienti candidati a terapia focale non può avvenire attraverso una biopsia prostatica trans rettale standard, dal momento che questa procedura non è sufficientemente accurata. Pertanto devono essere eseguite sia una biopsia perineale con almeno 24 prelievi che una risonanza magnetica multiparametrica. Questo perché bisogna essere assolutamente certi che il tumore prostatico sia monofocale. La presenza di due o più focolai di tumore all’ interno della ghiandola non consente la possibilità del trattamento focale. In particolare la biopsia perineale con utilizzo di “template” può consentire l’identificazione di focolai tumorali di 0,2 ml di volume con il 90% di accuratezza diagnostica. Pertanto, l’esatta localizzazione anatomica della lesione tumorale deve essere determinata con precisione. Il paziente che si sottopone a terapia focale deve seguire una accurata sorveglianza dopo il trattamento. In attesa di risultati di lungo termine, la terapia focale è attualmente considerata sperimentale.
Terapia ormonale (torna su)
Le cellule tumorali hanno bisogno di un “combustibile” per svilupparsi e sopravvivere. Questo combustibile è il testosterone, il principale ormone maschile. La terapia ormonale può agire o sopprimendo la concentrazione di testosterone nell’ organismo o inibendo la sua azione sulle cellule prostatiche. La terapia ormonale viene definita anche con altri termini sinonimi quali ormonoterapia, deprivazione androgenica o soppressione androgenica.
La terapia ormonale svolge un ruolo importante nelle fasi avanzate della malattia ma può essere impiegata anche prima, durante o dopo un trattamento radicale per migliorarne gli effetti. La maggior parte delle cellule tumorali risponde alla soppressione del testosterone. Tuttavia alcune cellule si sviluppano indipendentemente dal testosterone e non rispondono alla ormonoterapia. Inoltre, col passare del tempo aumentano le probabilità che cellule inizialmente sensibili a tale terapia diventino insensibili: in questi casi la malattia viene definita “resistente alla castrazione”.
Pertanto l’ormonoterapia non è un trattamento definitivo per il carcinoma prostatico. Tuttavia la terapia ormonale rimane un caposaldo importante nel tumore avanzato e nella progressione della malattia dopo trattamenti ad intento radicale quali chirurgia e radioterapia.
Difatti, nonostante una cospicua percentuale di paziente viene trattata in maniera definitiva, si stima che un 30% dei pazienti possono andare in progressione e sviluppare una malattia avanzata.
Sono qui di seguito descritte le forme più comuni di terapia ormonale. Anche se questa terapia è efficace nel controllare la progressione del tumore della prostata, è importante sottolineare che la soppressione del testosterone determina effetti secondari significativi in quasi tutti gli uomini.
Gli effetti collaterali possono essere i seguenti:
- Perdita della libido (desiderio sessuale)
- Vampate di calore
- Astenia (sensazione di stanchezza)
- Ginecomastia (ingrandimento delle mammelle)
- Mastodinia (dolore alle mammelle)
- Anemia (diminuzione del numero dei globuli rossi)
- Diminuzione del calcio nelle ossa
- Diminuzione della massa muscolare
Il tipo più semplice e più antico di ormonoterapia è rappresentato dall’orchiectomia, la rimozione chirurgica dei testicoli. Difatti, dal momento che circa il 90% del testosterone è prodotto nei testicoli, la loro ablazione chirurgica determina un abbattimento dei livelli ematici di questo ormone.
L’intervento è semplice, la convalescenza è rapida e non è necessaria nessuna ulteriore terapia. Questa procedura viene praticata da moltissimi anni ma è drastica ed irreversibile. Pertanto, la maggior parte dei pazienti opta per la terapia farmacologica. L’ orchiectomia rimane una opzione per i pazienti che preferiscono una terapia a basso costo praticata in un’unica soluzione.
I farmaci analoghi dell’LH agiscono sull’ LHRH, ormone chiave nella regolazione della produzione del testosterone. Il blocco della produzione dell’LHRH ottenuto tramite l’utilizzo di questi farmaci rappresenta la terapia ormonale più comune del tumore alla prostata. I farmaci appartenenti a questa categoria comprendono: leuprolide(Eligard,Enantone), il goserelin(Zoladex), il buserelin(Suprefact) e la triptorelina(Gonapeptyl,Decapeptyl). Vengono somministrati in singola dose una volta al mese, una volta ogni tre mesi o ogni sei mesi a seconda della formulazione. Una delle principali complicanze degli analoghi LHRH è il cosiddetto “flare up”, ossia un aumento transitorio iniziale del testosterone. Questo aumento può determinare un peggioramento dei sintomi del cancro della prostata quali il dolore osseo o l’aumento della frequenza e della difficoltà ad urinare.
Per questo motivo, nella fase iniziale del trattamento, gli analoghi dell’LH devono essere somministrati insieme con gli Antiandrogeni. Questa classe di farmaci include la bicalutamide (Casodex), la flutamide (Eulexin) e il ciproterone acetato (Androcur). Questi farmaci inibiscono l’azione del testosterone sulle cellule tumorali della prostata. Gli antiandrogeni vengono somministrati insieme agli analoghi per almeno le prime 4 settimane della terapia per impedire il “flare up”. La co-somministrazione di un analogo LH con un antiandrogeno viene definita Blocco Androgenico Totale (BAT). Gli antiandrogeni possono anche essere usati anche in monoterapia e non necessariamente insieme con gli analoghi. Gli antiandrogeni hanno il vantaggio di essere gravati da effetti secondari più lievi sulla vita sessuale, ma sono meno efficaci degli analoghi e dell’orchiectomia. La monoterapia con antiandorgeni pertanto non è indicata nelle fasi avanzate del tumore alla prostata. Negli ultimi anni sono stati sviluppati dei nuovi antiandrogeni di ultima generazione.
In particolare l’abiraterone acetato (Zytiga) è un farmaco in grado di inibire la produzione del testosterone non solo di provenienza testicolare ma anche quello prodotto dalle cellule surrenali e dalle stesse cellule tumorali. Viene utilizzato come terapia di seconda linea nel tumore prostatico metastatico resistente alla castrazione, ossia quando le cellule prostatiche tumorali non rispondono più alla soppressione del testosterone ottenuta con il blocco androgenico. L’enzalutamide (Xtendi) è invece un nuovo antiandrogeno con una affinità maggiore per il recettore del testosterone. Ha un meccanismo di azione simile a quello della flutamide e della bicalutamide ma un’efficacia superiore. Viene utilizzato se vi è una progressione di malattia dopo terapia con abiraterone.
Chemioterapia (torna su)
Il termine “chemioterapia” si riferisce a qualunque tipo di terapia che usi prodotti di derivazione chimica per uccidere o arrestare lo sviluppo delle cellule tumorali. I farmaci hanno svariati meccanismi di azione ma sono tutti basati sullo stesso semplice principio: impedire la divisione cellulare e lo sviluppo e la diffusione del tumore. Inizialmente, la chemioterapia è stata usata soltanto per alleviare i sintomi dell’adenocarcinoma prostatico avanzato e metastatico. Nel 2004 furono pubblicati due studi che dimostrarono l’efficacia del docetaxel(Taxotere) nel migliorare la sopravvivenza dei pazienti affetti da cancro della prostata resistente alla castrazione.
Il docetaxel è un farmaco chemioterapico appartenente alla famiglia dei taxani, che inibisce la proliferazione delle cellule tumorali. Di recente è stato sviluppato un nuovo taxano, il cabazitaxel, che viene oggi impiegato come terapia di seconda linea dopo il docetaxel. Altri farmaci di recente introduzione sono il sileupecel e il denosumab. Il sileupecel agisce migliorando la risposta immunologica dell’organismo contro le cellule tumorali. Il Denosumab è un anticorpo monoclonale che viene impiegato per la prevenzione della perdita della massa ossea nei pazienti affetti da metastasi ossee. Il Denosumab si è dimostrato superiore all’ acido zoledronico, il farmaco impiegato in precedenza per la stessa indicazione.
Grazie allo sviluppo di nuovi farmaci oggigiorno la sopravvivenza dei pazienti affetti da tumore alla prostata avanzato è aumentata di gran lunga, e questo tipo di patologia può essere considerata una malattia cronica.




